
特設サイト
診療紹介
高度急性期病院である当センターの主要診療科として、常に先進的医療を岐阜地域に提供するとともに、常に循環器救急患者を受け入れることが出来る体制を整えています。循環器領域のすべての分野において、非侵襲的検査(心電図検査、心エコー検査、心臓核医学検査、造影CT検査、心臓MR検査など)と心臓・血管カテーテル検査などの侵襲的検査とをバランスよく組み合わせて診断をし、薬物治療や生活習慣改善指導(包括的心臓リハビリテーション)を行うとともに、心臓・血管へのカテーテルによる治療、不整脈へのカテーテルアブレーション、ペースメーカー植込みなどの高度専門医療を行っています。2010年11月より併設した不整脈科は、小児循環器科、臨床工学士とともにチーム医療を推進しています。大血管、弁膜症疾患については、心臓血管外科と共同でハイブリット治療を行っており、2010年度から大動脈ステントグラフト留置術、2014年から経カテーテル的大動脈弁置換術(TAVI)、2019年から経皮的僧帽弁接合不全修復術(MitraClip)、2021年7月より経カテーテル左心耳閉鎖術(WATCHMAN)、2021年11月から経皮的卵円孔開存閉鎖術を開始しています。急性心筋梗塞、心不全、不整脈などの急性疾患に対しては、院内に常に循環器内科医を配置することにより、24時間体制で患者を受け入れ、常に緊急心臓カテーテル検査・治療ができる体制をとっています。救急医療を広く担うため、病診・病病連携を積極的にすすめて、外来は予約制とし、紹介患者、救急患者を中心とした医療を行っています。
診療内容
- 虚血性心疾患、不整脈疾患、心筋疾患、心臓弁膜症、心不全など心臓疾患
- 大動脈瘤、大動脈解離など大動脈疾患、下肢閉塞性動脈疾患など末梢血管疾患
- 高血圧、肺高血圧、肺塞栓症
- 成人先天性心疾患
- その他循環器疾患全般
主な対象疾患
虚血性心疾患:陳旧性心筋梗塞、狭心症など冠動脈の異常に伴う疾患
| 2019年 | 2020年 | 2021年 | 2022年 | 2023年 | |
|---|---|---|---|---|---|
| 経皮的冠動脈インターベンション | 478 | 394 | 470 | 470 | 448 |
| 緊急冠動脈インターベンション | 196 | 156 | 159 | 186 | 172 |
| 薬物溶出性ステント | 466 | 359 | 439 | 390 | 372 |
| ロータブレーター | 59 | 65 | 93 | 65 | 49 |
| エキシマレーザー冠動脈形成術 | 34 | 18 | 34 | 20 | 44 |
虚血性心疾患が疑われる症状や心電図異常が認められ、状態が安定している場合には、運動負荷または薬物負荷心筋シンチまたはMDCTを用いた冠動脈造影3D CTによりスクリーニングを行なったうえで、心臓カテーテル検査による冠動脈造影により診断をします。症状や心電図など非侵襲的検査から虚血性心疾患が強く疑われる場合は、すぐに心臓カテーテル検査を行なうこともあります。
症状が安定している症例で、冠動脈造影にて有意な狭窄が認められた場合には、個々の症例を総合的に判断し、薬物治療、経皮的冠動脈インターベンション(カテーテルによる治療)、冠動脈バイパス術の適応を決めています。また、境界領域の冠動脈狭窄病変に対しては、冠血流予備量比(FFR)を測定し、冠動脈インターベンションの適応について検討を行っています。
冠動脈インターベンションにおいては9割以上で血管内超音波検査(IVUS)を施行し、確実で丁寧な治療を心がけています。また、複雑な冠動脈病変の場合は、光干渉断層法(OCT)や血管内視鏡による冠動脈病変の観察を行って、最適な治療を選択しています。
石灰化が強く硬い、血栓量が多いなど冠動脈病変の形態により、ロータブレーター、エキシマレーザー、ダイアモンドバックなどの特殊なカテーテルデバイスによる治療を行っています。2023年6月からは石灰化病変に対して超音波を用いた衝撃波血管内砕石術(SHOCKWAVE)の使用も開始しました。
近年は末梢循環障害や末梢血管攣縮に伴う狭心症が注目されており、心臓カテーテル検査時に冠血流予備能(CMR)、冠微小血管抵抗指数(IMR)を測定して積極的に診断し、薬物治療に結びつけています。
急性冠症候群:急性心筋梗塞と不安定狭心症
24時間体制で患者を受け入れ、治療しています。ST上昇型心筋梗塞では、一刻も早く冠動脈再疎通をすることが重要であり、緊急冠動脈造影を施行し、血栓吸引、冠動脈形成術・ステント留置術による早期再灌流を施行しています。重症心不全合併症例に対しては機械的補助循環(IABP、PCPS、Impella)を適宜使用し、集中的に治療しています。
心大血管疾患リハビリテーション
| 2019年 | 2020年 | 2021年 | 2022年 | 2023年 | |
|---|---|---|---|---|---|
| 新規患者数 | 1,218 | 1,184 | 1,145 | 1,157 | 1,133 |
| 実施件数(年間延べ件数) | 14,097 | 12,707 | 13,941 | 10,272 | 10,006 |
心臓リハビリテーションは包括的心臓リハビリテーションを多職種チームで積極的に進めています。心肺運動負荷試験等により運動耐用能を評価して運動処方を行い、QOL(Quality of Life:生活の質)の改善をはかるとともに、再発予防のため危険因子の評価・治療を行っています。外来での集団リハビリテーションや心肺運動負荷検査も、新型コロナ感染症が5類となったのを機に、引き続き感染には十分配慮したうえで徐々に再開しています。
動脈疾患
| 2019年 | 2020年 | 2021年 | 2022年 | 2023年 | |
|---|---|---|---|---|---|
| 末梢動脈形成術 | 149 | 116 | 94 | 87 | 80 |
| 胸部大動脈ステントグラフト | 28 | 7 | 9 | 8 | 7 |
| 腹部大動脈ステントグラフト | 66 | 34 | 35 | 32 | 33 |
慢性閉塞性動脈硬化症に対しては、上肢下肢の血圧の比(ABI)でスクリーニングを行い、疑わしい場合は下肢動脈エコー、下肢動脈MRA、下肢動脈造影CT等にて診断をしています。基本的治療は薬物治療、リハビリテーションで、症状の強い症例に対してはカテーテル治療を行なっています。2016年より重症虚血肢の救肢のため、他科と連携して重症下肢虚血に対する下肢血行再建も積極的に行なっています。
胸腹部大動脈瘤に対しては2010年9月より心臓血管外科と共同で大動脈ステントグラフト内挿術を開始しています。大動脈瘤破裂に対する大動脈ステントグラフト留置術についても、心臓血管外科と適応を検討した上で緊急で施行しております。
構造的心疾患:弁膜症、心筋疾患
| 2018年 | 2019年 | 2020年 | 2021年 | 2022年 | 2023年 | |
|---|---|---|---|---|---|---|
| 経皮的大動脈弁置換術(TAVI) | 34 | 81 | 54 | 52 | 59 | 54 |
| 経皮的僧帽弁接合不全修復術 (MitraClip) | ー | 36 | 40 | 39 | 30 | 21 |
| 経カテーテル左心耳閉鎖術(WATCHMAN) | ー | ー | ー | 23 | 56 | 49 |
| 経皮的卵円孔開存閉鎖術 | ー | ー | ー | 5 | 27 | 10 |
弁膜症では、心エコー検査、心臓MR検査、造影CT検査など、様々なモダリティーを用いて診断、評価をして治療方針を決めています。2014年より重度大動脈弁狭窄症に対して経皮的大動脈弁置換術(TAVI)を開始しており、多職種によるハートチームで十分に検討したうえで適応を決めています。2019年より開始した、治療に難渋する心不全患者の僧帽弁閉鎖不全症に対する経皮的僧帽弁接合不全修復術(MitraClip)も、ハートチームで十分に検討したうえで適応を決め、積極的に行っています。また、2021年より心房細動症例で、消化管出血、血尿など出血性事象の発生リスクが高いため抗凝固療法の継続が困難な方や、抗凝固薬を内服していても血栓塞栓症を発症した方に対して経カテーテル左心耳閉鎖術(WATCHMAN)を開始し、順調に症例を重ねています。卵円孔開存を伴う潜因性の脳梗塞症例に対する経皮的卵円孔開存閉鎖術も、順調に施行できています。
不整脈
WPW症候群、発作性上室性頻拍症、心房細動(粗動)、心室性期外収縮などの頻脈性不整脈に対しては、薬物療法による発作予防を試みますが、近年は高周波カテーテルアブレーション(心筋焼灼術)による根治術が確立してきたことより、積極的にカテーテルアブレーションによる完治を追求しています。カルトシステムやエンサイトシステムも適宜使用しています。
失神、心不全の原因となる洞不全症候群、高度房室ブロックなどの徐脈性不整脈に対しては、緊急時には随時体外式ペースメーカーによる応急処置を行い、必要に応じてペースメーカー植え込み術を施行しています。2017年10月よりリードレスペースメーカー植込み(Micra)を、2021年11月より房室同期の可能なMicraAVの使用も開始し、適応を検討しながら積極的に使用しています。
心室細動、心室頻拍などの致死性心室性不整脈を有する症例に対しては、突然死を回避するための植込み型除細動器(ICD)植込みを行なっています。
心房細動に対しては、リスクを評価して脳梗塞などの塞栓症予防のためのダビガトラン、リバーロキサバン、アキビサバン、エドキサバンなどによる抗凝固療法を原則として施行しています。施行しています。発作性心房細動に対しては抗凝固処置を行ったうえで適宜除細動を施行し、持続性の場合は経食道心エコーにて左房内血栓の評価をしたうえで除細動の適応、時期を決めています。洞調律維持には、適応を検討し、積極的にカテーテルアブレーションを施行しています。また、個々の症例の病状に応じて高周波アブレーションまたは心筋冷凍焼灼術(クライオアブレーション)を選択しています。
心不全
現在、心不全患者は年々増加してきており、再発を繰り返して、徐々に悪化していく症例も多く、毎週、他職種による心不全チームのカンファレンスを開始し、再発予防に対する取り組みを開始しています。 急性心不全に対しては血管拡張剤、利尿剤、強心剤、心房性Naペプチドなどの薬物治療を行い、重症例では必要に応じて機械的補助循環(LABP、PCPS、Impella)、限外濾過(ECUM)による治療を行なっています。 慢性心不全では非侵襲的・侵襲的検査を組み合わせて病態・病因を解明し、レニン・アンギオテンシン系抑制薬、β遮断薬、利尿薬などを組み合わせて治療を行っています。また、難治性心不全に対しては適応を検討したうえで両室ペーシングによる心臓再同期療法(CRT)を行っています。
研究
冠動脈ステント、冠動脈形成術、超音波、心臓核医学、カテーテルアブレーションなどの研究を国内外の学会で発表するとともに、学術雑誌に発表しております。
関連する診療科・専門外来
その他
- 2013年8月よりエキシマレーザー冠動脈形成術を開始しました。
- 2013年夏よりハイブリッド手術室の運用を開始し、2014年4月より経カテーテル的大動脈弁置換術(TAVI)を開始しました。
- 2015年9月より、発作性心房細動に対するクライオアブレーションを開始しました。
- 2017年9月より、リードレスペースメーカ植込み術を開始しました。
- 2019年5月より、経皮的僧帽弁接合不全修復術(Mitra Clip)を開始しました。
- 2020年5月より、経カテーテル左心耳閉鎖術(WATCHMAN)を開始しました。
- 2021年5月より、経カテーテル左心耳閉鎖術(WATCHMAN)を開始しました。
- 2021年11月より、経皮的卵円孔開存閉鎖術を開始しました。
経皮的大動脈弁置換術(TAVI)
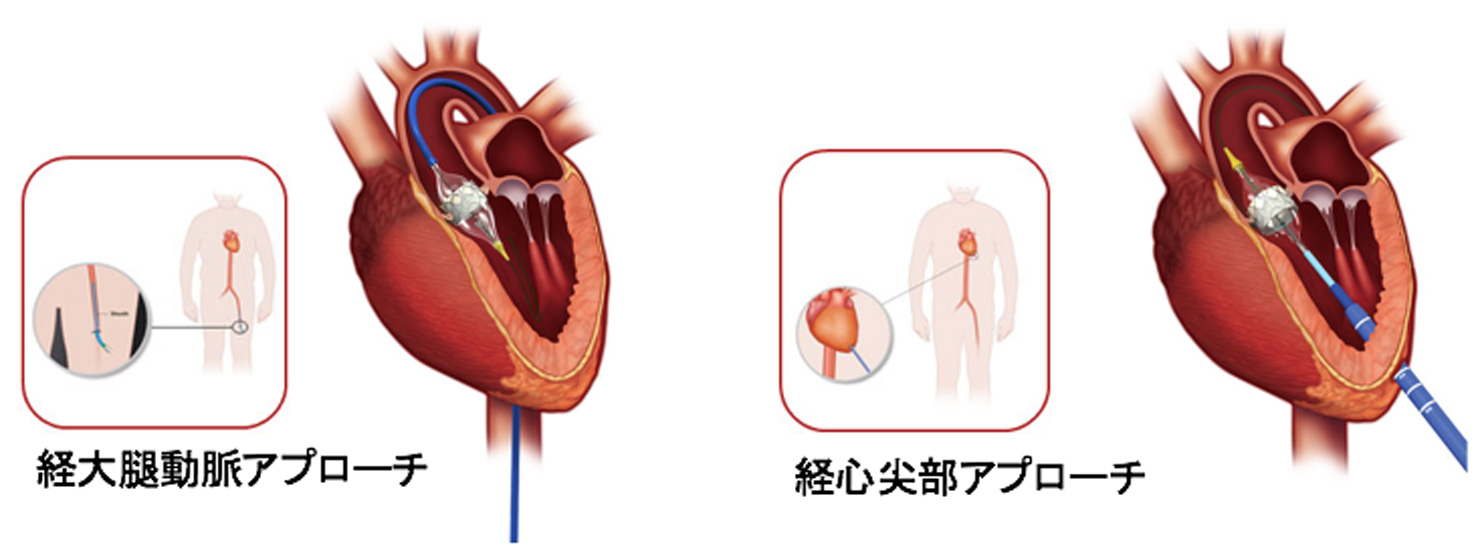
大動脈弁狭窄症は左心室と大動脈の間にある大動脈弁が硬くなって、開きが悪くなり、全身に十分な血液が送ることができなくなる病気で、心不全の原因となります。根本的治療は弁を取り換える開胸手術(弁置換術)がゴールデンスタンダードです。しかし、高齢で体力が低下している、または併存疾患のためハイリスクで開胸手術が困難な患者さんを対象に、カテーテルを使って人工弁を患者さんの心臓に留置する治療法が経皮的大動脈弁置換術です。太ももの付け根の血管から挿入する「経大腿アプローチ」を第一選択とし、足からの挿入が困難な場合は肋骨の間を小さく切開し、心臓の先端(心尖部)から挿入する「経心尖アプローチ」で行います。

経皮的僧帽弁接合不全修復術(MitraClip)
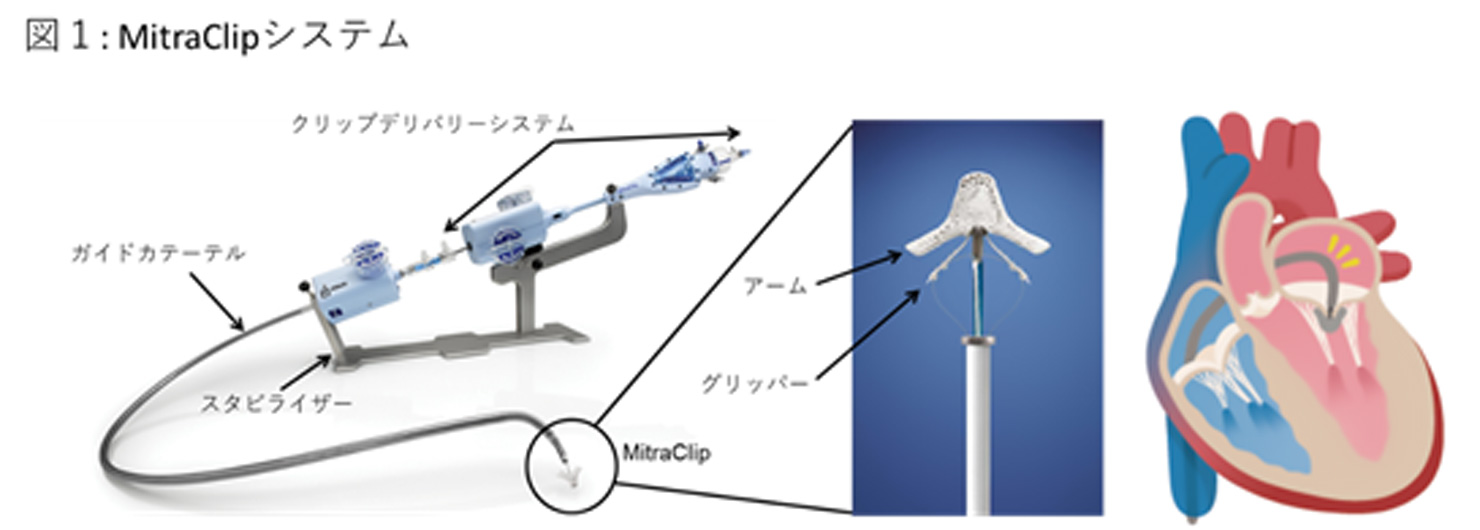
僧帽弁閉鎖不全症とは左心房と左心室の間にある一方向弁の僧帽弁が何らかの原因で適切に閉じないことで、全身へ行くべき血液が左心室から左心房へ逆流する病気で、心不全の原因となります。僧帽弁閉鎖不全症に対する治療は、従来開胸を伴う外科的手術(弁置換術・弁形成術)が一般的ですが、高齢な方や多数の併存疾患のために外科的手術がハイリスクと判断された場合は、手術を断念せざるを得ない場合が少なくありませんでした。
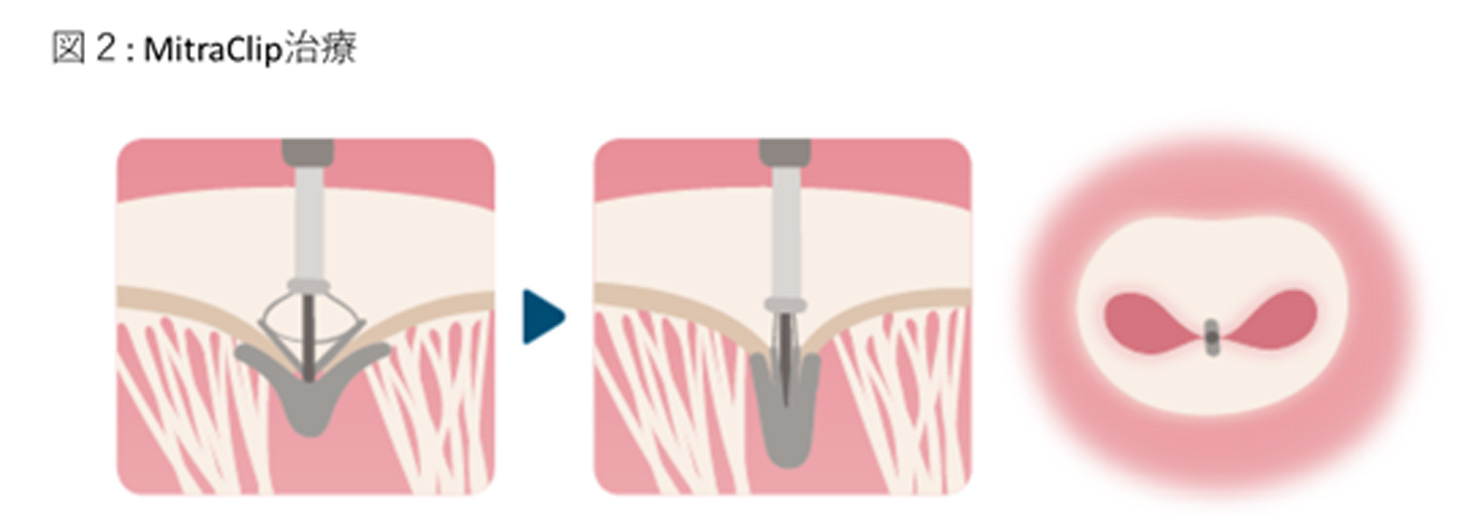
そのような方々に対象として、足の付け根の血管(大腿静脈)からカテーテルを挿入し、Clipを心臓内へ運び、逆流している僧帽弁をClipでつまむことで、僧帽弁閉鎖不全症を制御する治療法が経皮的僧帽弁接合不全修復術です。
経皮的左心耳閉鎖術(WATCHMAN)
心房細動は心房が細かく震えることで起こる不整脈の一つです。心房が細かく震えると心房の中で血液がよどみ、心房の中、特に左心耳で血の塊(血栓)が形成されやすくなります(図1)。血栓が脳の血管に到達すると脳梗塞を発症します。心房細動患者さんでは脳卒中のリスクが5倍高くなるとされます。脳梗塞のうち30%が心原性とされ、その90%以上が左心耳からの血栓とされています。また、日本における心房細動の有病率は約1%、70代以上の有病率は約3%で、高齢者ほどかかりやすく、現在ではcommon diseaseの一つと考えられています。心房細動による脳梗塞を予防するためには抗凝固薬が有効ですが、出血リスクが増大するというデメリットがあります。
WATCHMANは左心耳を閉鎖することで脳梗塞発症リスクを軽減し、一方、抗凝固薬から離脱することができ出血リスクも軽減できるデバイスです(写真1)。大腿静脈を穿刺するのみで、全身麻酔で1.5-2時間、そのうちのカテーテル操作時間は0.5-1時間と短く、負担の少ない手技です(図2)。手技前日に入院し、入院日含み3泊4日と短い入院期間で実施が可能です。
WATCHMANの適応
脳梗塞発症リスクが高く、長期にわたり抗凝固療法が必要な方のうち、以下の項目が1つ以上当てはまる、出血リスクが高い方が対象となります。
- HAS-BLEDスコア(心房細動患者に対する出血リスクの評価方法)が3以上
- 転倒に伴う外傷に対して治療を必要とした既往が複数回ある
- びまん性脳アミロイド血栓症の既往
- 抗血小板薬の2剤以上の併用が長期(1年以上)にわたって必要
- 出血学術研究協議会(BARC)のタイプ3に該当する大出血の既往
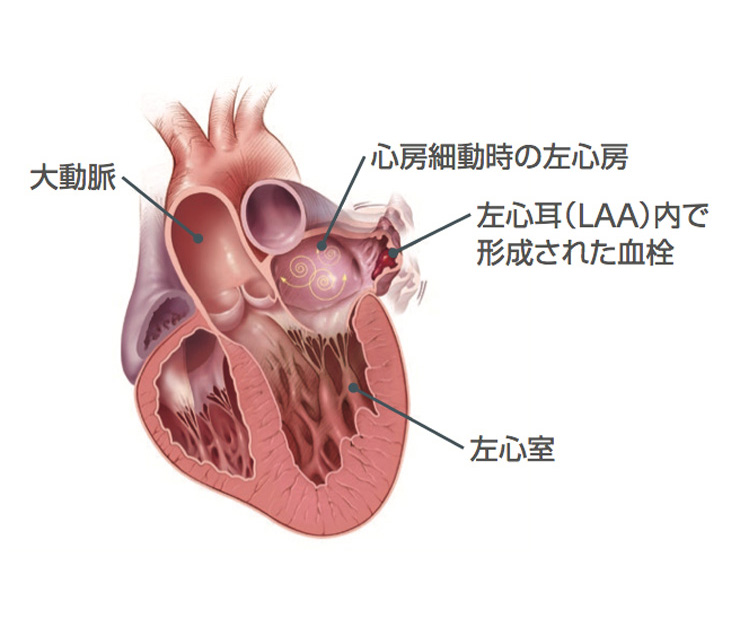
図1:左心耳で形成される血栓

写真1:WATCHMAN(ボストン・サイエンティフィックジャパン株式会社)
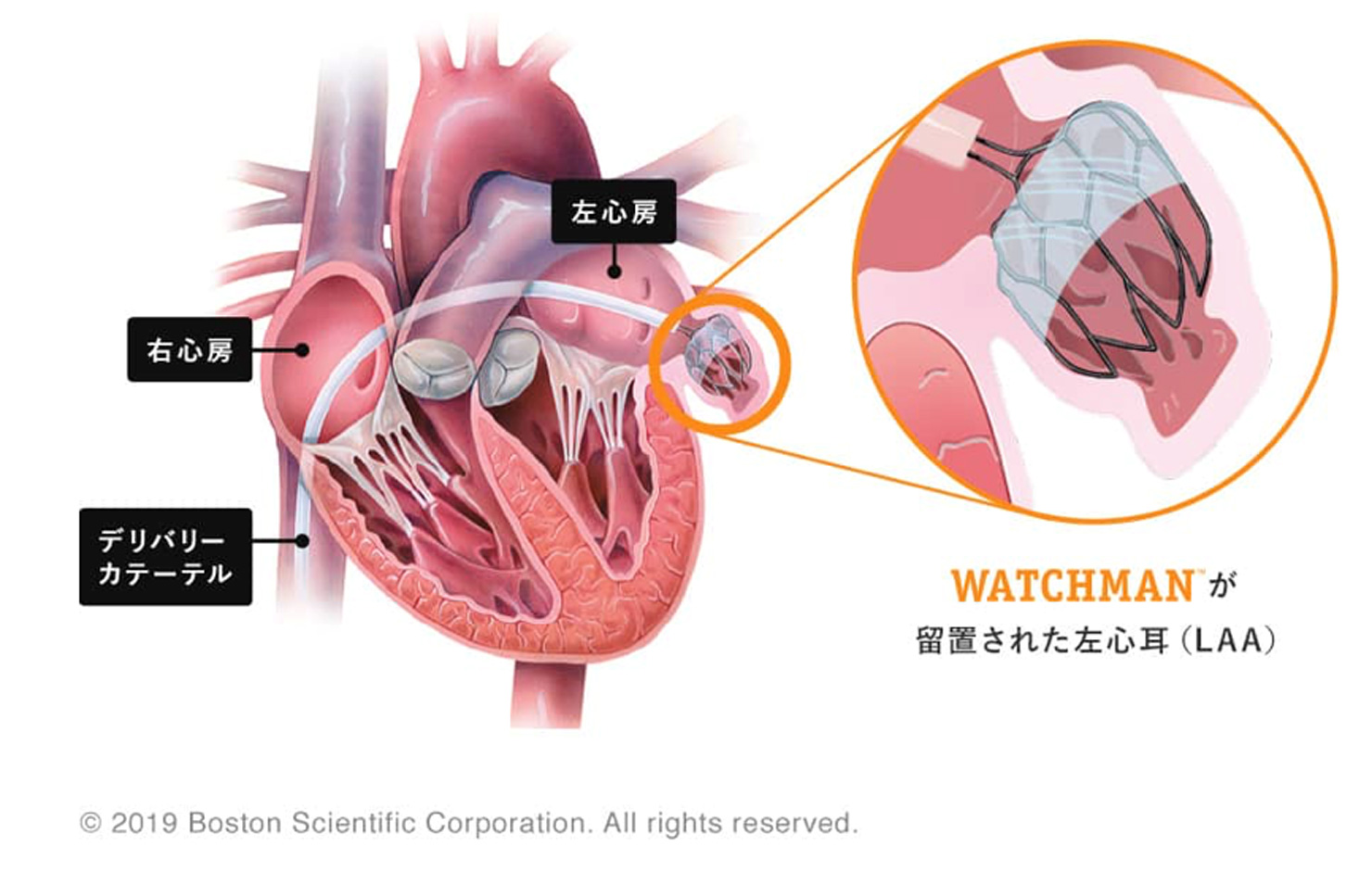
図2:WATCHMAN留置中の様子
経皮的卵円孔開存閉鎖術
心臓の心房中隔(右心房と左心房を分ける壁)は胎児の頃には孔(卵円孔)が空いており、多くの方は出産後に閉鎖します。この孔があいている状態を卵円孔開存と呼びます(図1)。卵円孔開存は健康な成人でも20-25%程度認め、通常は自覚症状や生命予後に影響を与えることありませんが、足の静脈などに血の塊(血栓))ができ、それが心臓まで流れていくと、開存した卵円孔を介して右心房から左心房へ流れ、脳血管へ到達して脳梗塞を発症することがあります(図2)。脳梗塞の原因としてはラクナ梗塞が25%、アテローム血栓性が25%、心原性が25%、潜因性が25%、その他が5%程度と報告されています。潜因性とは、『脳血管や心臓について調べてみたものの、原因がはっきりしないもの』とされます。卵円孔開存の診断は通常の経胸壁心エコーでは診断が困難のため、見落とされることが多く、経食道心エコーなどで詳しく調べると、潜因性の半分は卵円孔開存が関係している可能性があることが報告されています。特に60歳未満の若い方の脳梗塞の場合可能性が高くなり、精密な検査が望ましいとされています。
卵円孔開存に対するカテーテル治療
卵円孔開存による脳梗塞の再発を抑えるには
- 薬物療法
- 開胸術による卵円孔閉鎖
- カテーテルによる卵円孔閉鎖(図3)
が選択肢となります。2019年12月より国内で卵円孔開存に対してデバイスを用いて閉鎖するカテーテル治療が適応となり、薬物療法単独よりも、脳梗塞の再発予防効果が高いことが臨床試験で示され、国内で普及しつつあります。大腿静脈を穿刺するのみで、全身麻酔で1.0-1.5時間、そのうちのカテーテル操作時間は30-45分と短く、負担の少ない手技です。手技前日に入院し、入院日含み3泊4日と短い入院期間で実施が可能です。
卵円孔開存閉鎖術の適応
卵円孔開存の関与があり得る潜因性脳梗塞の診断基準に合致した方
脳梗塞が『卵円孔開存の関与があり得るかどうか』の診断は脳梗塞の専門科や循環器の専門科が協議する必要があります。当院では脳梗塞の担当医師と循環器内科医師で組織されるブレインハートカンファレンスを定期的に実施しています。
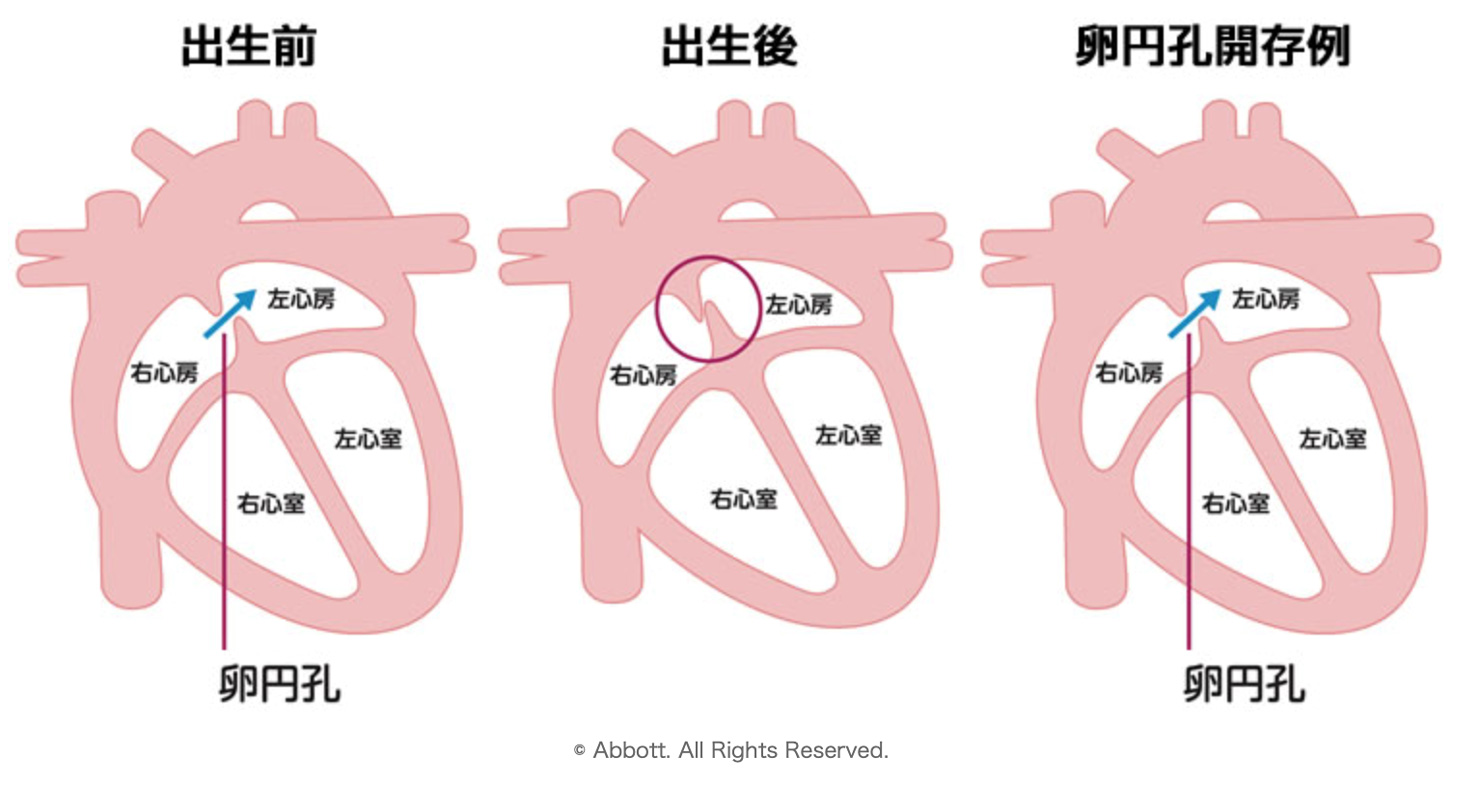
図1:卵円孔開存のイメージ図
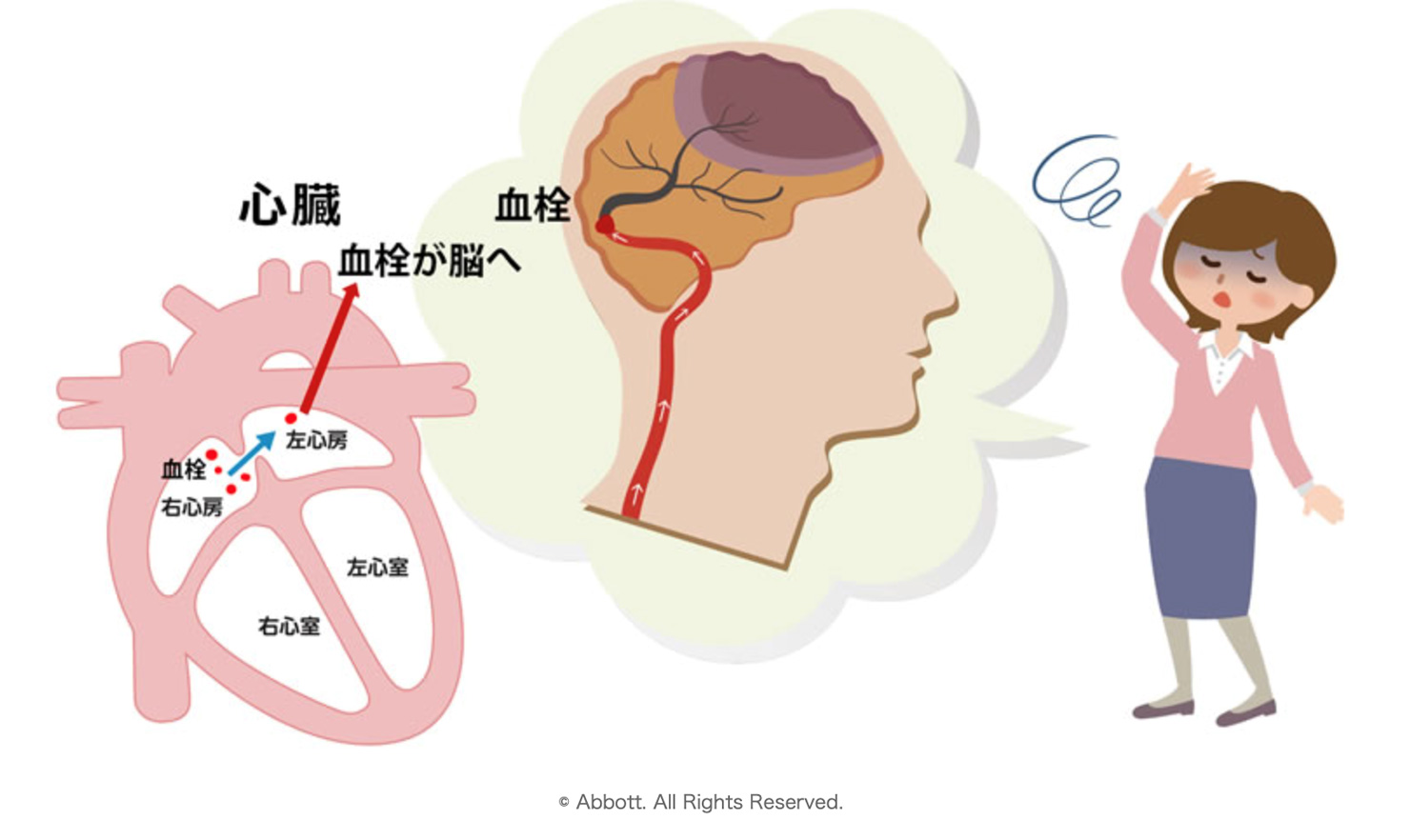
図2:卵円孔開存を介した脳梗塞のイメージ
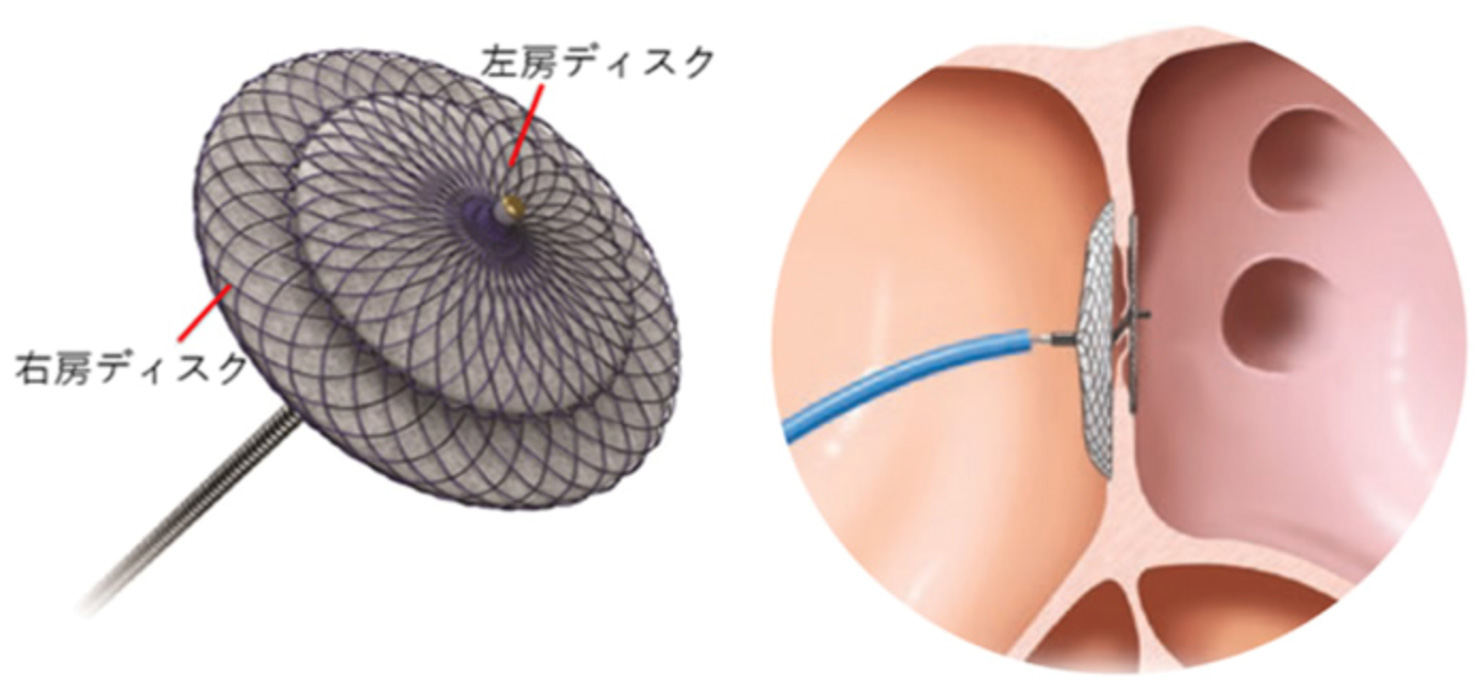
図3:カテーテルでの卵円孔開存閉鎖デバイスのイメージ図
あらい まさずみ
荒井 正純
| 役職 |
|
|---|---|
| 認定資格 |
|

のだ としゆき
野田 俊之
| 役職 |
|
|---|---|
| 認定資格 |
|
たにはた しんたろう
谷畠 進太郎
| 役職 |
|
|---|---|
| 認定資格 |
|
いわま まこと
岩間 眞
| 役職 |
|
|---|---|
| 認定資格 |
|
もりした けんたろう
森下 健太郎
| 役職 |
|
|---|---|
| 認定資格 |
|
いいだ まみ
飯田 真美
| 役職 |
|
|---|---|
| 認定資格 |
|
わりた しゅんいちろう
割田 俊一郎
| 役職 |
|
|---|---|
| 認定資格 |
|
かとう たかし
加藤 崇
| 役職 |
|
|---|---|
| 認定資格 |
|
やがさき ひろと
矢ケ﨑 裕人
| 役職 |
|
|---|---|
| 認定資格 |
|
わたなべ りょうた
渡邊 亮太
| 役職 |
|
|---|---|
| 認定資格 |
|
うえの たかひろ
上野 貴弘
| 役職 |
|
|---|---|
| 認定資格 |
|
ほりお しゅんたろう
堀尾 俊太郎
| 役職 |
|
|---|---|
| 認定資格 |
|
おおしま よしたけ
大島 功丈
| 役職 |
|
|---|---|
| 認定資格 |
|
わたなべ けいたろう
渡邊 啓太郎
| 役職 |
|
|---|---|
| 認定資格 |
|
かみたに けい
上谷 渓
| 役職 |
|
|---|---|
| 認定資格 |
|
むとう こうすけ
武藤 功甫
| 役職 |
|
|---|---|
| 認定資格 |
|
たなか りゅうたろう
田中 隆太郎
| 役職 |
|
|---|
こばやし はやた
小林 隼大
| 役職 |
|
|---|
かのう よしたろう
加納 嘉太郎
| 役職 |
|
|---|
たかはし としはる
高橋 寿治
| 役職 |
|
|---|
わたなべ さちろう
渡辺 佐知郎
| 役職 |
|
|---|---|
| 認定資格 |
|
外来担当医表
| 月曜日 | 火曜日 | 水曜日 | 木曜日 | 金曜日 | ||
|---|---|---|---|---|---|---|
| 1診 | 午前 | ー | ー | 渡邊啓太郎 (初診・再診) |
武藤功甫 (再診) |
ー |
| 午後 | 第①週 担当医 (ペースメーカー) |
第①週 担当医 (ペースメーカー) |
第①週 担当医 (ペースメーカー) |
第①週 担当医 (ペースメーカー) |
加藤崇 (初診・再診) |
|
| 2診 | 午前 | 森下健太郎 (初診・再診) |
渡辺佐知郎 (初診・再診) |
荒井正純 (初診・再診) |
矢ケ崎裕人 (初診・再診) |
渡辺佐知郎 (初診・再診) |
| 午後 | 森下健太郎 (再診) |
渡辺佐知郎 (再診) |
荒井正純 (再診) |
矢ケ崎裕人 |
渡辺佐知郎 (再診) |
|
| 3診 | 午前 | 野田俊之 (初診・再診) |
上谷渓 (初診・再診) |
野田俊之 (初診・再診) |
野田俊之 (初診・再診) |
割田俊一郎 (初診・再診) |
| 午後 | 野田俊之 (再診) |
上谷渓 (再診) |
野田俊之 (再診) |
野田俊之 (再診) |
割田俊一郎 (ICD外来) |
|
| 4診 | 午前 | 岩間眞 (初診・再診) |
荒井正純 (初診・再診) |
岩間眞 (初診・再診) |
堀尾俊太郎 (初診・再診) |
田中隆太郎 (初診・再診) |
| 午後 | 岩間眞 (再診) |
荒井正純 (再診) |
岩間眞 (再診) |
堀尾俊太郎 (再診) |
荒井正純 (再診) |
|
| 5診 | 午前 | 渡邊亮太 (初診・TAVI外来) |
割田俊一郎 (初診・再診) |
大島功丈 (初診・再診) |
加藤崇 (初診・再診) |
上野貴弘 (初診・再診) |
| 午後 | 渡邊亮太 (再診) |
割田俊一郎 (再診) |
大島功丈 (再診) |
加藤崇 (脚外来) (再診) |
上野貴弘 (再診) |
|
※病診予約は、赤字部分で可能です。 水曜日午後野田医師、金曜日午後加藤医師は病診予約可能です。
診療実績
入院・外来患者数
| 2019年 | 2020年 | 2021年 | 2022年 | 2023年 | |
|---|---|---|---|---|---|
| 年間入院患者数(人) | 21,596 | 20,163 | 20,912 | 16,996 | 17,484 |
| 平均在院日数(日) | 6.5 | 7.2 | 6.8 | 7.3 | 7.1 |
| 外来患者数(人) | 31,710 | 26,509 | 27,146 | 26,193 | 26,148 |
| 1日外来患者数(人/日) | 131.0 | 109.1 | 112.2 | 107.8 | 111.7 |
検査件数
| 疾患名 | 2019年 | 2020年 | 2021年 | 2022年 | 2023年 |
|---|---|---|---|---|---|
| 冠動脈造影検査 | 981 | 797 | 727 | 768 | 831 |
| 冠動脈CT | 677 | 471 | 637 | 716 | 554 |
| 心筋シンチグラム | 1,512 | 1,482 | 1,624 | 1,513 | 1,164 |
| 心臓MRI | 344 | 330 | 155 | 168 | 168 |
| 経胸壁心エコー検査 | 18,483 | 17,197 | 17,394 | 17,894 | 17,305 |
| 経食道心エコー検査 | 692 | 605 | 698 | 758 | 810 |









